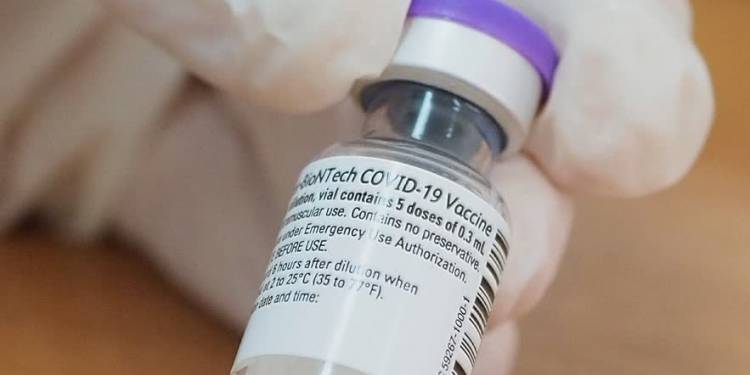
Europejska Agencja Leków rozpoczęła ocenę szczepionek dla młodzieży od 12 do 15 lat produkcji BioNTech i Pfizer. Konsorcjum złożyło w ubiegłym tygodniu wniosek o rozszerzenie zezwolenia na stosowanie preparatów, które obecnie są dostępne dla osób powyżej 16 roku życia.
Europejska Agencja Leków poinformowała, że przeprowadzi przyspieszoną ocenę danych przysłanych przez BioNTech i Pfizer, w tym także wyników badań klinicznych z udziałem nastolatków. Opinia ma być opublikowana w czerwcu. Unijna agencja zastrzegła, że termin ogłoszenia oceny może być przesunięty, jeśli potrzebne będą dodatkowe informacje od konsorcjum. Zgodnie z procedurami ocena ekspertów unijnej agencji zostanie przekazana Komisji Europejskiej, która wydaje ostateczne decyzje o dopuszczeniu szczepionek na unijny rynek.
CZYTAJ: W Polsce ruszą badania kliniczne nad stosowaniem szczepionki przeciw COVID u dzieci
Konsorcjum BioNTech i Pfizer poinformowało w ubiegłym tygodniu, że wniosek do Europejskiej Agencji Leków został złożony w oparciu o wyniki III fazy badań klinicznych, które wykazały 100-procentową skuteczność preparatu u młodzieży od 12 do 15 lat. Testy przeprowadzone zostały na grupie ponad 2 tysięcy nastolatków.
Rzecznik Ministerstwa Zdrowia Wojciech Andrusiewicz poinformował też w piątek, że Polska jest jednym z czterech państw, w których w najbliższym czasie firma Pfizer BioNTtech będzie prowadzić badania w zakresie możliwości szczepień od 6. miesiąca życia do 12. roku życia.
RL / PAP / opr. ToMa
Fot. archiwum