– Zakończyły się badania kliniczne dotyczące szczepionek przeciw COVID-19 dla dzieci od 12 do 15 roku życia – powiedział w środę prezes Urzędu Rejestracji Produktów Leczniczych, Wyrobów Medycznych i Produktów Biobójczych dr Grzegorz Cessak.
– Badania były prowadzone w kilku krajach, w tym w Stanach Zjednoczonych. Wiadomo, że szczepionka jest skuteczna i bezpieczna, a niepożądane odczyny poszczepienne (NOP) mają łagodniejszy przebieg niż u dorosłych. Szczepionka jest skuteczna także na nowe mutacje koronawirusa – dodał.
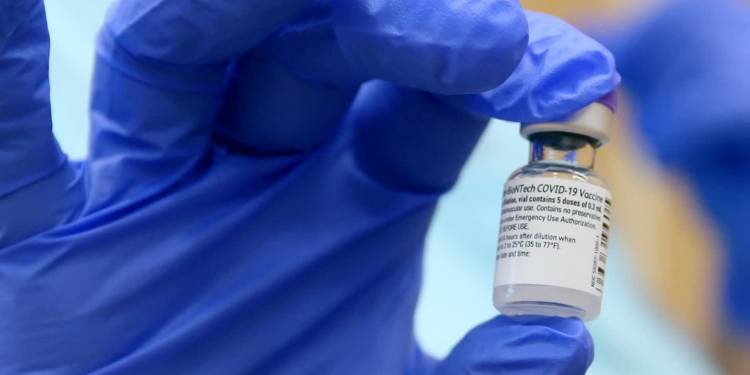
W przyszłym tygodniu szczepionkę przeciwko koronawirusowi Pfizer/BioNTech dla dzieci w wieku od 12 do 15 lat ma zatwierdzić Amerykańska Agencja ds. Żywności i Leków (FDA). Żeby preparat mógł być stosowany w Europie, musi przejść ocenę Europejskiej Agencji Leków (EMA). – O ile nie zostanie zgłoszona przez EMA potrzeba złożenia dodatkowych danych i wyjaśnień, końcowa rekomendacja Europejskiej Agencji Leków może pojawić się w czerwcu – powiedział dr Cessak.
Na dzień dzisiejszy dopuszczona do obrotu w Europie jest szczepionka dla młodzieży od 16 do 18 roku życia, która przeszła procedurę rejestracyjną Europejskiej Agencji Leków (EMA). Szczepienie przeciw COVID-19 dla tej grupy zostało uznane za skuteczne i bezpieczne.
Dr Cessak podkreślił, że badania z udziałem pacjentów pediatrycznych podlegają wnikliwej i krytycznej ocenie europejskich ekspertów współpracujących z Komitetem Pediatrycznym EMA. – Należy jednoznacznie stwierdzić, że w zakresie ustalonych kryteriów nie odnotowano istotnych różnic pomiędzy pacjentami pediatrycznymi i dorosłymi. Nie zaobserwowano żadnych dodatkowych ani nowych zdarzeń niepożądanych – powiedział.
Przypomniał, że Polska jest jednym z państw, w których Urząd Rejestracji Produktów Leczniczych zatwierdził również badania kliniczne w zakresie stosowania szczepionki firmy Pfizer od 6 miesiąca życia, do 12 roku życia, które rozpoczęły się pod koniec kwietnia. – Faza II/III badań klinicznych oceni bezpieczeństwo, tolerancję i immunogenność z grupą kontrolną otrzymującą placebo, przy wybranym poziomie dawki z fazy I badania klinicznego. W całym badaniu weźmie udział około 4500 dzieci z ośrodków w USA, Hiszpanii, Finlandii i Polski – powiedział dr Cessak.
Podkreślił, że priorytetem w szczepieniach są na razie osoby dorosłe. – Dopiero jak zaszczepimy osoby dorosłe, będą podejmowane kolejne decyzje: najpierw o szczepieniu młodzieży od 16 roku życia, a potem, po zatwierdzeniu zmiany przez EMA, kolejnych grup wiekowych – powiedział.
Jak informuje resort zdrowia, decyzje dotyczące rozszerzenia szczepień na młodsze roczniki zapadną w drugiej połowie maja.
RL / PAP / opr. ToMa
Fot. archiwum